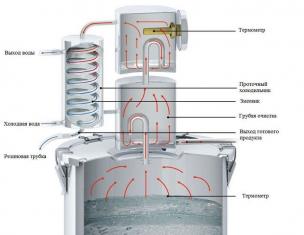
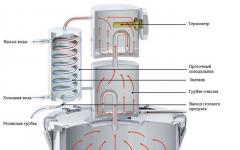
Электрохимический ряд активности металлов (ряд напряжений, ряд стандартных электродных потенциалов) - последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ 0 , отвечающих полуреакции восстановления катиона металла Me n+ : Me n+ + nē → Me
Практическое использование ряда активности металлов
Ряд напряжений используется на практике для сравнительной оценки химической активности металлов в реакциях с водными растворами солей и кислот и для оценки катодных и анодных процессов при электролизе:
- Металлы, стоящие левее водорода, являются более сильными восстановителями, чем металлы, расположенные правее: они вытесняют последние из растворов солей. Например, взаимодействие Zn + Cu 2+ → Zn 2+ + Cu возможно только в прямом направлении.
- Металлы, стоящие в ряду левее водорода, вытесняют водород при взаимодействии с водными растворами кислот-неокислителей; наиболее активные металлы (до алюминия включительно) - и при взаимодействии с водой.
- Металлы, стоящие в ряду правее водорода, с водными растворами кислот-неокислителей при обычных условиях не взаимодействуют.
- При электролизе металлы, стоящие правее водорода, выделяются на катоде; восстановление металлов умеренной активности сопровождается выделением водорода; наиболее активные металлы (до алюминия) невозможно при обычных условиях выделить из водных растворов солей.
Самыми активными считаются щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.
Какую информацию можно получить из ряда напряжений?
Ряд напряжений металлов широко используется в неорганической химии. В частности, результаты многих реакций и даже возможность их осуществления зависят от положения некоторого металла в ЭРН. Обсудим этот вопрос подробнее.
Взаимодействие металлов с кислотами
Металлы, находящиеся в ряду напряжений левее водорода, реагируют с кислотами - неокислителями. Металлы, расположенные в ЭРН правее Н, взаимодействуют только с кислотами - окислителями (в частности, с HNO 3 и концентрированной H 2 SO 4).
Пример 1 . Цинк расположен в ЭРН левее водорода, следовательно, способен реагировать практически со всеми кислотами:
Zn + 2HCl = ZnCl 2 + H 2
Zn + H 2 SO 4 = ZnSO 4 + H 2
Пример 2 . Медь находится в ЭРН правее Н; данный металл не реагирует с "обычными" кислотами (HCl, H 3 PO 4 , HBr, органические кислоты), однако вступает во взаимодействие с кислотами-окислителями (азотная, концентрированная серная):
Cu + 4HNO 3 (конц.) = Cu(NO 3) 2 + 2NO 2 + 2H 2 O
Cu + 2H 2 SO 4 (конц.) = CuSO 4 + SO 2 + 2H 2 O
Обращаю внимание на важный момент: при взаимодействии металлов с кислотами-окислителями выделяется не водород, а некоторые другие соединения. Подробнее об этом можно почитать !
Взаимодействие металлов с водой
Металлы, расположенные в ряду напряжений левее Mg, легко реагируют с водой уже при комнатной температуре с выделением водорода и образованием раствора щелочи.
Пример 3 . Натрий, калий, кальций легко растворяются в воде с образованием раствора щелочи:
2Na + 2H 2 O = 2NaOH + H 2
2K + 2H 2 O = 2KOH + H 2
Ca + 2H 2 O = Ca(OH) 2 + H 2
Металлы, расположенные в ряду напряжений от водорода до магния (включительно), в ряде случаев взаимодействуют с водой, но реакции требуют специфических условий. Например, алюминий и магний начинают взаимодействие с Н 2 О только после удаления оксидной пленки с поверхности металла. Железо не реагирует с водой при комнатной температуре, но взаимодействует с парами воды. Кобальт, никель, олово, свинец практически не взаимодействуют с H 2 O не только при комнатной температуре, но и при нагревании.
Металлы, расположенные в правой части ЭРН (серебро, золото, платина) не реагируют с водой ни при каких условиях.
Взаимодействие металлов с водными растворами солей
Речь пойдет о реакциях следующего типа:
металл (*) + соль металла (**) = металл (**) + соль металла (*)
Хотелось бы подчеркнуть, что звездочки обозначают в данном случае не степень окисления, не валентность металла, а просто позволяют различить металл № 1 и металл № 2.
Для осуществления подобной реакции необходимо одновременное выполнение трех условий:
- соли, участвующие в процессе, должны растворяться в воде (это легко проверить, пользуясь таблицей растворимости);
- металл (*) должен находиться в ряду напряжений левее металла (**);
- металл (*) не должен реагировать с водой (что тоже легко проверяется по ЭРН).
Пример 4 . Рассмотрим несколько реакций:
Zn + CuSO 4 = ZnSO 4 + Cu
K + Ni(NO 3) 2 ≠
Первая реакция легко осуществима, все перечисленные выше условия выполнены: сульфат меди растворим в воде, цинк находится в ЭРН левее меди, Zn не реагирует с водой.
Вторая реакция невозможна, т. к. не выполнено первое условие (сульфид меди (II) практически не растворяется в воде). Третья реакция неосуществима, поскольку свинец - менее активный металл, нежели железо (находится правее в ЭРН). Наконец, четвертый процесс НЕ приведет к осаждению никеля, поскольку калий реагирует с водой; образовавшийся гидроксид калия может вступить в реакцию с раствором соли, но это уже совершенно другой процесс.
Процесс термического распада нитратов
Напомню, что нитраты - это соли азотной кислоты. Все нитраты разлагаются при нагревании, но вот состав продуктов разложения может быть разным. Состав определяется положением металла в ряду напряжений.
Нитраты металлов, расположенных в ЭРН левее магния, при нагревании образуют соответствующий нитрит и кислород:
2KNO 3 = 2KNO 2 + O 2
В ходе термического разложения нитратов металлов, расположенных в ряду напряжений от Mg до Cu включительно, образуются оксид металла, NO 2 и кислород:
2Cu(NO 3) 2 = 2CuO + 4NO 2 + O 2
Наконец, при разложении нитратов наименее активных металлов (расположенных в ЭРН правее меди) образуются металл, диоксид азота и кислород.
Разность потенциалов «вещество электрода – раствор» как раз и служит количественной характеристикой способности вещества (как металлов, так и неметаллов) переходить в раствор в виде ионов, т.е. характери стикой ОВ способности иона и соответствующего ему вещества.
Такую разность потенциалов называют электродным потенциалом .
Однако прямых методов измерений такой разности потенциалов не существует, поэтому условились их определять по отношению к так называемому стандартному водородному электроду, потенци ал которого условно принят за ноль (часто его также называют электродом сравнения). Стандартный водородный электрод состоит из платиновой пластинки, погруженной в раствор кислоты с кон центрацией ионов Н + 1 моль/л и омываемой струей газообразного водорода при стандартных условиях .
Возникновение потенциала на стандартном водородном электроде можно представить себе следующим образом. Газообразный водород, адсорбируясь платиной, переходит в атомарное состояние:
H 2 2H .
Между атомарным водородом, образующимся на поверхности пластины, ионами водорода в растворе и платиной (электроны!) реализуется состояние динамического равновесия:
H Н + + е.
Суммарный процесс выражается уравнением:
Н 2 2Н + + 2е.
Платина не принимает участия в окислительно – восстанов ительном процессе, а является лишь носителем атомарного водорода.
Если пластинку некоторого металла, погруженную в раствор его соли с концентрацией ионов металла, равной 1 моль/л, соединить со стандартным водородным электродом, то получится гальванический элемент. Электродвижущая сила этого элемента (ЭДС), измеренная при 25° С, и характеризует стандартный электродный потенциал металла, обозначаемый обычно как Е 0 .
По отношению к системе Н 2 /2Н + некоторые вещества будут вести себя как окислители, другие - как восстановители. В настоящее время получены стандартные потенциалы практически всех металлов и многих неметаллов, которые характеризуют относительную способность восстановителей или окислителей к отдаче или захвату электронов.
Потенциалы электродов, выступающих как восстановители по отношению к водороду, имеют знак “-“, а знаком “+” отмечены потенциалы электродов, являющихся окислителями.
Если расположить металлы в порядке возрастания их стандартных электродных потенциалов, то образуется так называемый электрохимический ряд напряжений металлов :
Li , Rb , К, Ва, Sr , Са, N а, М g , А l , М n , Zn , С r , F е, С d , Со, N i , Sn , Р b , Н, Sb , В i , С u , Hg , А g , Р d , Р t , А u .
Ряд напряжений характеризует химические свойства металлов.
1. Чем более отрицателен электродный потенциал металла, тем больше его восстановительная способность.
2. Каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые стоят в ряду напряжений металлов после него. Исключениями являются лишь щелочные и щелочноземельные металлы, которые не будут восстанавливать ионы других металлов из растворов их солей. Это связано с тем, что в этих случаях с большей скоростью протекают реакции взаимодействия металлов с водой.
3. Все металлы, имеющие отрицательный стандартный электродный потенциал, т.е. находящиеся в ряду напряжений металлов левее водорода, способны вытеснять его из растворов кислот.
Необходимо отметить, что представленный ряд характеризует поведение металлов и их солей только в водных растворах, поскольку потенциалы учитывают особенности взаимодействия того или иного иона с молекулами растворителя. Именно поэтому электрохимический ряд начинается литием, тогда как более активные в химическом отношении рубидий и калий находятся правее лития. Это связано с исключительно высокой энергией процесса гидратации ионов лития по сравнению с ионами других щелочных металлов.
Алгебраическое значение стандартного окислительно-восстановительного потенциала характеризует окислительную активность соответствующей окисленной формы. Поэтому сопоставление значений стандартных окислительно-восстановительных потенциалов позволяет ответить на вопрос: протекает ли та или иная окислительно-восстановительная реакция?
Так, все полуреакции окисления галогенид-ионов до свободных галогенов
2 Cl – – 2 e = С l 2 Е 0 = -1,36 В (1)
2 Br – -2е = В r 2 E 0 = -1,07 В (2)
2I – -2 е = I 2 E 0 = -0,54 В (3)
могут быть реализованы в стандартных условиях при использовании в качестве окислителя оксида свинца ( IV ) (Е 0 = 1,46 В) или перманганата калия (Е 0 = 1,52 В). При использовании дихромата калия ( E 0 = 1,35 В) удается осуществить только реакции (2) и (3). Наконец, использование в качестве окислителя азотной кислоты ( E 0 = 0,96 В) позволяет осуществить только полуреакцию с участием иодид-ионов (3).
Таким образом, количественным критерием оценки возможности протекания той или иной окислительно-восстановительной реакции является положительное значение разности стандартных окислительно-восстановительных потенциалов полуреакций окисления и восстановления.
Вспомните:
Простые вещества состоят из атомов одного химического элемента, их разделяют на металлы и неметаллы;
Для металлов характерны металлический блеск, электропроводность, пластичность и т. п.
Понятие о ряде активности металлов
Во многих химических реакциях принимают участие простые вещества, в частности металлы. Металлы могут взаимодействовать почти со всеми классами неорганических соединений, которые изучаются в школьном курсе химии. Однако разные металлы проявляют разную активность в химических взаимодействиях, и от этого зависит, произойдет реакция или нет.
Чем больше активность металла, тем энергичнее он взаимодействует с другими веществами. По активности все металлы можно расположить в ряд, который называется рядом активности металлов (вытеснительным рядом металлов, рядом напряжений металлов, электрохимическим рядом напряжений металлов). Этот ряд впервые составил и изучил выдающийся украинский ученый Н. Н. Бекетов, поэтому у данного ряда есть еще одно название — ряд Бекетова.
Ряд активности металлов Бекетова выглядит так (более полный ряд см. на форзаце 2):
Русский и украинский химик, основатель украинской школы физической химии, академик Петербургской академии наук с 1886 г. Родился в семье морского офицера. Закончил Казанский университет, работал в Петербурге в Медико-химической лаборатории.

Преподавал химию цесаревичу — будущему императору Николаю II. С 1855 г. профессор императорского университета в Харькове, где по предложению ученого в 1864 г. было открыто первое в Украине физикохимическое отделение. Именно там впервые в мире он начал преподавать физическую химию как отдельную дисциплину. Бекетов открыл способ восстановления металлов из их оксидов, который и сегодня используют в металлургии, установил зависимость сродства элементов от порядкового номера, первым получил чистые оксиды щелочных элементов (Натрия, Калия), составил ряд активности металлов, который назван его именем, был автором первого в мире учебника по физической химии.
В этом ряду металлы расположены по уменьшению их химической активности в водных растворах. Таким образом, среди приведенных металлов наиболее активным является калий, а наименее активным — золото. С помощью этого ряда легко выяснить, какой металл активнее другого. Также в этом ряду находится водород. Конечно, водород не является металлом, но в данном ряду его активность принята за точку отсчета (своего рода ноль).
Взаимодействие металлов с кислотами
Металлы, расположенные в ряду активности слева от водорода, способны вступать в реакции с кислотами, в которых атомы металлических элементов замещают атомы Гидрогена в кислотах. При этом образуются соль соответствующей кислоты и водород H 2 (рис. 36.1, с. 194):

Чем левее расположен металл в ряду активности, тем более бурно он взаимодействует с кислотами. Наиболее интенсивно вытесняют водород из кислот те металлы, которые расположены в самом начале ряда. Так, магний взаимодействует очень бурно (жидкость словно

закипает), цинк взаимодействует значительно спокойнее, железо реагирует совсем слабо (пузырьки водорода едва образуются), а медь вовсе не взаимодействует с кислотой (рис. 36.2).
Если металл расположен в ряду активности справа от водорода, то он не способен вытеснять водород из растворов кислот, и потому реакция не происходит (табл. 12, с. 197):
![]()
Обратите внимание на уравнения реакций металлов с кислотами, приведенные выше: в этих реакциях атомы металлических элементов из простого вещества замещают атомы Гидрогена в кислотах. Такие реакции называют реакциями замещения.
Реакции замещения — это реакции, в которых атом элемента простого вещества вытесняет атом другого элемента из сложного вещества.
Взаимодействие нитратной и концентрированной сульфатной кислот с металлами происходит по другой схеме. В таких реакциях водород почти не выделяется, а выделяются другие продукты реакции, о чем вы узнаете в следующих классах.
Взаимодействие металлов с водой
Металлы, расположенные в ряду активности слева от водорода, способны вытеснять водород не только из растворов кислот, но и из воды. Как и в случае с кислотами, активность взаимодействия металлов с водой зависит от расположения металла в ряду активности (рис. 36.3).
Металлы, расположенные в ряду активности слева от магния, взаимодействуют с водой при обычных условиях. В таких реакциях образуются щелочи и водород:

Литий взаимодействует с водой очень бурно (рис. 36.4):
Калий реагирует с водой так бурно, что иногда случается взрыв: во время реакции выделяется настолько большое количество теплоты, что выделяемый водород загорается и вызывает воспламенение самого металла.

Кальций и натрий взаимодействуют с водой так же бурно, но без взрыва:

То, что в результате реакции активных металлов с водой образуются щелочи, можно доказать, добавив раствор фенолфталеина, который приобретает характерную малиновую окраску (рис. 36.5, с. 196).


Магний взаимодействует с водой по такой же схеме, что и активные металлы, но вместо щелочи образуется нерастворимое основание. Реакция протекает настолько медленно, что сначала при добавлении магния к воде никакой реакции не наблюдается — пузырьки водорода начинают выделяться лишь спустя некоторое время (рис. 36.6). Для инициирования реакции воду следует немного подогреть или проводить реакцию в кипящей воде.
Большинство других металлов, расположенных между магнием и водородом в ряду активности, также могут взаимодействовать с водой (вытеснять из нее водород), но это происходит при более «жестких» условиях: для этого через раскаленные металлические опилки пропускают перегретый водяной пар. Конечно, при таких условиях гидроксиды разлагаются (на оксид и воду), поэтому продуктами реакции являются оксид соответствующего металлического элемента и водород:

Никель, олово и свинец пассивируются водой, поэтому ни при каких условиях с водой не реагируют.
Таблица 12. Зависимость химических свойств металлов от положения в ряду активности
|
K Ca Na Mg |
Al Zn Fe |
Ni Sn Pb |
Cu Ag Hg Au |
|
|
^ Активность металлов увеличивается |
||||
|
Реагируют с кислотами с образованием соли и водорода |
Не реагируют с кислотами |
|||
|
Реагируют с водой при обычных условиях |
Вытесняют водород из воды при высокой температуре, образуют оксиды |
С водой не взаимодействуют |
||
|
Из водного раствора соли металл вытеснить невозможно |
Металл можно получить вытеснением его более активным металлом из раствора соли |
|||
Взаимодействие металлов с солями
Если соль растворима в воде, то металлический элемент в ней может быть вытеснен более активным металлом:
Например, если погрузить в раствор купрум(П) сульфата железную пластинку, через определенное время на ней выделится медь в виде красного налета:
Со временем железная пластинка покрывается довольно плотным слоем порошка меди, а раствор светлеет, что свидетельствует об уменьшении в нем концентрации купрум(П) сульфата (рис. 36.7).

Железо расположено в ряду активности слева от меди, поэтому атомы Феррума могут вытеснить атомы Купрума из соли. Но если в раствор купрум(П) сульфата погрузить серебряную пластину, то реакция не происходит:
CuSO 4 + Ag ф
Медь можно вытеснить из соли любым металлом, расположенным слева от меди в ряду активности металлов. При этом
Рис. 36.8. Менее активное, чем медь, серебро оседает на поверхности медной проволоки. Раствор приобретает голубую окраску благодаря образованию на нем соли Купрума

медь будет вытеснять из растворов других солей любой металл, который расположен в ряду активности справа от нее (рис. 36.8):
Наиболее активные металлы, расположенные в самом начале ряда,— натрий, калий — не вытесняют другие металлы из растворов солей, поскольку они такие активные, что взаимодействуют не с растворенной солью, а с водой, в которой эта соль растворена.
Взаимодействие металлов с оксидами
Оксиды металлических элементов также способны взаимодействовать с металлами. Более активные металлы вытесняют менее активные из оксидов. Но, в отличие от взаимодействия металлов с солями, чтобы реакция осуществилась, оксиды необходимо расплавить:

Для получения металла из оксида можно применять любой металл, который расположен в ряду активности левее, даже самые активные натрий и калий, ведь в расплавленном оксиде воды нет:

Вытеснение металлов из солей или оксидов более активными металлами иногда применяют в промышленности для получения металлов.
Многие кислоты и другие вещества алхимики называли «спиртами» (от латин. spiritus — «дух», «запах»). Так, был spiritus sale — соляный спирт, или хлоридная кислота, spiritus nitrate — нитратная кислота и т. д. В современном химическом языке от этих названий остались только spiritus ammonia — нашатырный спирт, который является раствором аммиака NH 3 , и spiritus vini — винный, или этиловый, спирт.
Горящие активные металлы (магний, натрий и др.) невозможно погасить водой. Причина заключается в том, что при контакте с водой горящий магний реагирует с ней, вследствие чего выделяется водород, который только усиливает горение.
. «Царской водкой» химики называют кислоту, которая является смесью концентрированных нитратной и хлоридной кислот. Такое название эта смесь получила потому, что с ней взаимодействует даже золото.
Взаимодействие хлоридной кислоты с металлами
Оборудование: штатив с пробирками.
Реактивы: гранулированные образцы металлов: железо, цинк, олово, алюминий, медь; хлоридная кислота.
Правила безопасности:
Остерегайтесь попадания реактивов на одежду, кожу, в глаза; в случае попадания кислоты ее следует немедленно смыть большим количеством воды и протереть место разбавленным раствором соды.
1. В отдельные пробирки поместите выданные вам кусочки металлов (железо, цинк, олово, алюминий, медь).
2. Прилейте в каждую пробирку по 1-2 мл хлоридной кислоты. Что вы наблюдаете? С каким металлом выделение водорода проходит наиболее интенсивно?
3. Запишите свои наблюдения в тетрадь.
4. Сделайте вывод о возможности взаимодействия металлов с кислотами. Сопоставьте активность этого взаимодействия с положением металла в ряду активности.
Взаимодействие металлов с солями в водном растворе
Оборудование: штатив с пробирками.
Реактивы: растворы купрум(П) сульфата, плюмбум(П) нитрата; железная и цинковая пластинки.
Правила безопасности:
Используйте небольшие количества реактивов;
Остерегайтесь попадания реактивов на одежду, кожу, в глаза; в случае попадания вещества его следует немедленно смыть водой.
1. В первую пробирку налейте раствор купрум(П) сульфата, во вторую — раствор плюмбум(П) нитрата.
2. В первую пробирку с купрум(П) сульфатом погрузите железную пластину, а во вторую — цинковую. Что наблюдаете? Изменятся ли признаки реакции, если в раствор купрум(П) сульфата опустить цинковую пластину, а в раствор плюмбум(П) нитрата — железную пластину? А если бы в обоих случаях использовали серебряную пластину?
3. Запишите свои наблюдения. Составьте соответствующие уравнения реакций.
4. Сделайте вывод, в котором обоснуйте возможность взаимодействия солей с металлами с точки зрения положения металлов в ряду активности.
Выводы
1. Все металлы, расположенные в один ряд по уменьшению их активности, образуют ряд активности металлов. В него также добавлен водород как вещество, относительно которого определяют активность металлов.
2. Металлы, расположенные в ряду активности слева от водорода, вытесняют его из кислот и воды. Чем левее расположен металл, тем активнее он вступает в реакции. Металлы слева от магния взаимодействуют с водой при обычных условиях, образуя соответствующие гидроксиды и водород, а металлы, расположенные от магния до водорода, взаимодействуют с водой при высокой температуре с образованием оксидов.
3. Металлы могут вытеснять друг друга из соли или оксида: более активный металл всегда вытесняет менее активный. Для проведения таких реакций с водными растворами солей нельзя использовать металлы, расположенные в ряду активности до магния, поскольку они будут взаимодействовать с водой, а не с растворенной в ней солью.
Контрольные вопросы
1. Какую информацию содержит ряд активности металлов Бекетова? По какому принципу в нем расположены металлы?
2. Какие металлы вытесняют водород из кислот? Приведите примеры.
3. Какие металлы взаимодействуют с водой? Какие из них взаимодействуют при обычных условиях, а какие — при высокой температуре?
4. По какому принципу необходимо отбирать металлы для вытеснения других металлов из растворов солей? из расплавов оксидов?
Задания для усвоения материала
1. При каких условиях кислоты реагируют: а) с металлами; б) основаниями; в) солями? Ответ подтвердите уравнениями реакций.
2. При каких условиях соли реагируют: а) с кислотами; б) металлами; в) основаниями? Ответ подтвердите уравнениями реакций.
3. Кусочки магния и олова поместили в раствор хлоридной кислоты. В каком случае реакция протекает интенсивнее? Составьте уравнения этих реакций.
4. Образцы натрия, кальция и цинка залили водой. Что наблюдается в каждом случае? Составьте соответствующие уравнения реакций.
5. В раствор никель(И) сульфата погрузили свинцовую и железную пластины. В каком случае реакция происходит? Ответ обоснуйте.
6. Почему для получения меди из раствора купрум(П) сульфата нельзя использовать натрий и калий, ведь они активнее меди? Можно ли их использовать для добывания меди из расплава купрум(И) оксида?
7. Калий взаимодействует с водой настолько бурно, что выделяемый водород загорается. Какое вещество образуется в растворе? Составьте уравнение реакции.
8. Предложите, как с помощью химических реакций разделить смесь меди и железа.
9. Какие вещества образуются при взаимодействии воды: а) с активными металлами; б) оксидами активных металлических элементов; в) оксидами неметаллических элементов? Приведите примеры.
10. Составьте уравнения возможных реакций:

11. С какими из данных веществ взаимодействует сульфатная кислота: NaNO 3 , CO 2 , NaOH, AgNO 3 , Zn, Ba, CaCO 3 , Cu(OH) 2 , Zn(OH) 2 , HCl, SiQ 2 , Fe 2 O 3 , Hg? Составьте уравнения реакций.
12. Какие из указанных веществ взаимодействуют с водой: Na, Ba, Fe, Fe 2 O 3 , H 2 SO 4 , NaOH, CaO, ZnО? Ответ подтвердите уравнениями реакций.
13. При погружении цинковой пластины в раствор купрум(іі) нитрата на пластине выделилась медь массой 3,2 г. Определите массу цинка, который растворился в результате реакции.
14. Вычислите массу олова, которое можно получить в результате взаимодействия станнум(іі) оксида с алюминием массой 0,54 кг.
15. Какой объем водорода (н. у.) выделится, если цинк массой 97,5 г полностью прореагирует с хлоридной кислотой?
16. Какое количество вещества сульфатной кислоты необходимо для взаимодействия с магнием массой 12 г? Какая масса соли при этом образуется? Какой объем газа (н. у.) выделится?
17. Какое количество вещества меди можно выделить из раствора купрум(іі) сульфата, содержащего 32 г этой соли?
18. Смесь магния массой 6 г и железа массой 16,8 г обработали достаточным количеством раствора сульфатной кислоты. Какой объем водорода (н. у.) выделился в результате реакции?
19. В раствор аргентум(І) нитрата массой 85 г с массовой долей соли 2 % погрузили цинковую пластинку. Вычислите массу серебра, которое выделится на пластинке после окончания реакции. Определите, как изменится масса пластинки по сравнению с ее исходной массой.
20 5 . Алюминий — достаточно активный металл, но изделия из алюминия хранятся на воздухе без видимых признаков порчи. Если зачищенное изделие из алюминия, например ложку или вилку, на некоторое время поместить в раствор меркурий(іі) нитрата, оно покроется серебристым налетом. Обработанное таким образом изделие при хранении на воздухе за довольно короткое время превращается в серый порошок, среди которого можно наблюдать серебристые шарики. Объясните с химической точки зрения, почему могут происходить такие изменения. Составьте соответствующие уравнения реакций.
Это материал учебника
Гроссе Э., Вайсмантель X.
Химия для любознательных. Основы химии и занимательные опыты.
Глава 3 (продолжение)НЕБОЛЬШОЙ КУРС ЭЛЕКТРОХИМИИ МЕТАЛЛОВ
Мы уже познакомились с электролизом растворов хлоридов щелочных металлов и получением металлов с помощью расплавов. Сейчас попробуем на нескольких несложных опытах изучить некоторые закономерности электрохимии водных растворов, гальванических элементов, а также познакомиться с получением защитных гальванических покрытий.Электрохимические методы применяются в современной аналитической химии, служат для определения важнейших величин теоретической химии.
Наконец, коррозия металлических предметов, которая наносит большой урон народному хозяйству, в большинстве случаев является электрохимическим процессом.
РЯД НАПРЯЖЕНИЯ МЕТАЛЛОВ
Основополагающим звеном для понимания электрохимических процессов является ряд напряжения металлов. Металлы можно расположить в ряд, который начинается с химически активных и заканчивается наименее активными благородными металлами:Li, Rb, К, Ва, Sr, Са, Mg, Al, Be, Mn, Zn, Cr, Ga, Fe, Cd, Tl, Co, Ni, Sn, Pb, H, Sb, Bi, As, Cu, Hg, Ag, Pd, Pt, Au .
Так выглядит, по новейшим представлениям, ряд напряжений для важнейших металлов и водорода. Если из двух любых металлов ряда изготовить электроды гальванического элемента, то на предшествующем в ряду материале появится отрицательное напряжение.
Величина напряжения (электрохимический потенциал ) зависит от положения элемента в ряду напряжении и от свойств электролита.
Сущность ряда напряжения установим из нескольких простых опытов, для которых нам понадобятся источник тока и электрические измерительные приборы. Растворим около 10 г кристаллического сульфата меди в 100 мл воды и погрузим в раствор стальную иглу или кусочек железной жести. (Рекомендуем предварительно до блеска зачистить железо тонкой наждачной шкуркой.) Через короткое время железо покроется красноватым слоем выделившейся меди. Более активное железо вытесняет медь из раствора, причем железо растворяется в виде ионов, а медь выделяется в виде металла. Процесс продолжается до тех пор, пока раствор находится в контакте с железом. Как только медь покроет всю поверхность железа, он практически прекратится. В этом случае образуется довольно пористый слой меди, так что защитные покрытия без применения тока получать нельзя.
В следующих опытах опустим в раствор сульфата меди небольшие полоски цинковой и свинцовой жести. Через 15 минут вытащим их, промоем и исследуем под микроскопом. Мы различим красивые, похожие на ледяные, узоры, которые в отраженном свете имеют красную окраску и состоят из выделившейся меди. Здесь также более активные металлы перевели медь из ионного в металлическое состояние.
В свою очередь, медь может вытеснять металлы, стоящие ниже в ряду напряжений, то есть менее активные. На тонкую полоску листовой меди или на расплющенную медную проволоку (предварительно зачистив поверхность до блеска) нанесем несколько капель раствора нитрата серебра. Невооруженным взглядом можно будет заметить образовавшийся черноватый налет, который под микроскопом в отраженном свете имеет вид тонких игл и растительных узоров (так называемых дендритов).
Чтобы выделить цинк без тока, необходимо применить более активный металл. Исключая металлы, которые бурно взаимодействуют с водой, находим в ряду напряжений выше цинка магний. Несколько капель раствора сульфата цинка поместим на кусок магниевой ленты или на тонкую стружку электрона. Раствор сульфата цинка получим, растворив кусочек цинка в разбавленной серной кислоте. Одновременно с сульфатом цинка добавим несколько капель денатурата. На магнии через короткий промежуток времени заметим, особенно под микроскопом, выделившийся в виде тонких кристалликов цинк.
В общем, любой член ряда напряжения может быть вытеснен из раствора, где он находится в виде иона, и переведен в металлическое состояние. Однако при испытании всевозможных комбинаций, нас может постичь разочарование. Казалось бы, если полоску алюминия погрузить в растворы солей меди, железа, свинца и цинка, на ней должны выделяться эти металлы. Но этого, однако, не происходит. Причина неудачи кроется не в ошибке в ряду напряжений, а основана на особом торможении реакции, которое в данном случае обусловлено тонкой оксидной пленкой на поверхности алюминия. В таких растворах алюминий называют пассивным.
ЗАГЛЯНЕМ ЗА КУЛИСЫ
Чтобы сформулировать закономерности протекающих процессов, мы можем ограничиться рассмотрением катионов, а анионы исключить, так как они сами в реакции не участвуют. (Правда, на скорость осаждения влияет вид анионов.) Если для простоты предположить, что и выделяющийся и растворенный металлы дают двухзарядные катионы, то можно записать:Me 1 + Me 2 2+ = Ме 1 2+ + Ме 2
Причем для первого опыта Ме 1 = Fe, Me 2 = Сu.
Итак, процесс состоит в обмене зарядами (электронами) между атомами и ионами обоих металлов. Если отдельно рассматривать (в качестве промежуточных реакций) растворение железа или осаждение меди, то получим:
Fe = Fe 2+ + 2е --
Сu 2+ + 2е -- = Сu
Теперь рассмотрим случай, когда металл погружен в воду или в раствор соли, с катионом которой обмен невозможен из-за его положения в ряду напряжений. Несмотря на это, металл стремится перейти в раствор в виде иона. При этом атом металла отдает два электрона (если металл двухвалентный), поверхность погруженного в раствор металла заряжается по отношению к раствору отрицательно, а на границе раздела образуется двойной электрический слой. Эта разность потенциалов препятствует дальнейшему растворению металла, так что процесс вскоре приостанавливается.
Если в раствор погрузить два различных металла, то они оба зарядятся, но менее активный - несколько слабее, в силу того, что его атомы менее склонны к отщеплению электронов.
Соединим оба металла проводником. Вследствие разности потенциалов поток электронов потечет от более активного металла к менее активному, который образует положительный полюс элемента. Протекает процесс, при котором более активный металл переходит в раствор, а катионы из раствора выделяются на более благородном металле.
Проиллюстрируем теперь несколькими опытами приведенные выше несколько абстрактные рассуждения (которые к тому же представляют собой грубое упрощение).
Сначала наполним химический стакан вместимостью 250 мл до середины 10%-ным раствором серной кислоты и погрузим в нее не слишком маленькие куски цинка и меди. К обоим электродам припаяем или приклепаем медную проволоку, концы которой не должны касаться раствора.
Пока концы проволоки не соединены друг с другом, мы будем наблюдать растворение цинка, которое сопровождается выделением водорода. Цинк, как следует из ряда напряжения, активнее водорода, поэтому металл может вытеснять водород из ионного состояния. На обоих металлах образуется двойной электрический слой. Разность потенциалов между электродами проще всего обнаружить с помощью вольтметра. Непосредственно после включения прибора в цепь стрелка укажет примерно 1 В, но затем напряжение быстро упадет. Если подсоединить к элементу маленькую лампочку, потребляющую напряжение 1 В, то она загорится - сначала довольно сильно, а затем накал станет слабым.
По полярности клемм прибора можно сделать вывод, что медный электрод является положительным полюсом. Это можно доказать и без прибора, рассмотрев электрохимию процесса. Приготовим в маленьком химическом стакане или в пробирке насыщенный раствор поваренной соли, добавим примерно 0,5 мл спиртового раствора индикатора фенолфталеина и погрузим оба замкнутых проволокой электрода в раствор. Около отрицательного полюса будет наблюдаться слабое красноватое окрашивание, которое вызвано образованием на катоде гидроксида натрия.
В других опытах можно помещать в ячейку различные пары металлов и определять возникающее напряжение. Например, магний и серебро дадут особенно большую разность потенциалов благодаря значительному расстоянию между ними ряду напряжений, а цинк и железо, наоборот, очень маленькую, менее десятой доли вольта. Применяя алюминий, мы не получим из-за пассивации практически никакого тока.
Все эти элементы, или, как говорят электрохимики, цепи, имеют тот недостаток, что при съемке тока на них очень быстро падает напряжение. Поэтому электрохимики всегда измеряют истинную величину напряжения в обесточенном состоянии с помощью метода компенсации напряжения, то есть сравнивая его с напряжением другого источника тока.
Рассмотрим процессы в медно-цинковом элементе несколько подробнее. На катоде цинк переходит в раствор по следующему уравнению:
Zn = Zn 2+ + 2е --
На медном аноде разряжаются ионы водорода серной кислоты. Они присоединяют электроны, поступающие по проволоке от цинкового катода и в результате образуются пузырьки водорода:
2Н + + 2е -- = Н 2
Через короткий промежуток времени медь покроется тончайшим слоем пузырьков водорода. При этом медный электрод превратится в водородный, а разность потенциалов уменьшится. Этот процесс называют поляризацией электрода. Поляризацию медного электрода можно устранить, добавив в ячейку после падения напряжения немного раствора дихромата калия. После этого напряжение опять увеличится, так как дихромат калия окислит водород до воды. Бихромат калия действует в этом случае как деполяризатор.
На практике применяют гальванические цепи, электроды которых не поляризуются, или цепи, поляризацию которых можно устранить, добавив деполяризаторы.
В качестве примера неполяризуемого элемента рассмотрим элемент Даниэля, который раньше часто использовали как источник тока. Это тоже медно-цинковый элемент, но оба металла погружены в различные растворы. Цинковый электрод помещается в пористой глиняной ячейке, наполненной разбавленной (примерно 20%-ной) серной кислотой. Глиняную ячейку подвешивают в большом стакане, в котором находится концентрированный раствор сульфата меди, а на дне - слой кристаллов сульфата меди. Вторым электродом в этом сосуде служит цилиндр из медного листа.
Этот элемент можно изготовить из стеклянной банки, имеющейся в продаже глиняной ячейки (в крайнем случае используем цветочный горшок, закрыв отверстие в дне) и двух подходящих по размеру электродов.
В процессе работы элемента цинк растворяется с образованием сульфата цинка, а на медном электроде выделяются ионы меди. Но при этом медный электрод не поляризуется и элемент дает напряжение около 1 В. Собственно, теоретически напряжение на клеммах составляет 1,10 В, но при съеме тока мы измеряем несколько меньшую величину, вследствие электрического сопротивления ячейки.
Если мы не снимем ток с элемента, нужно вытащить цинковый электрод из раствора серной кислоты, потому что иначе он будет растворяться с образованием водорода.
Схема простой ячейки, для которой не требуется пористой перегородки, показана на рисунке. Цинковый электрод расположен в стеклянной банке наверху, а медный - вблизи дна. Вся ячейка наполнена насыщенным раствором поваренной соли. На дно банки насыплем горсть кристаллов сульфата меди. Образующийся концентрированный раствор сульфата меди будет смешиваться с раствором поваренной соли очень медленно. Поэтому при работе элемента на медном электроде будет выделяться медь, а в верхней части ячейки будет растворяться цинк в виде сульфата или хлорида.
Сейчас для батарей используют почти исключительно сухие элементы, которые более удобны в употреблении. Их родоначальником является элемент Лекланше. Электродами служат цинковый цилиндр и угольный стержень. Электролит представляет собой пасту, которая в основном состоит из хлорида аммония. Цинк растворяется в пасте, а на угле выделяется водород. Чтобы избежать поляризации, угольный стержень опускают в полотняный мешочек со смесью из угольного порошка и пиролюзита. Угольный порошок увеличивает поверхность электрода, а пиролюзит действует как деполяризатор, медленно окисляя водород.
Правда, деполяризующая способность пиролюзита слабее, чем у упоминавшегося ранее дихромата калия. Поэтому при получении тока в сухих элементах напряжение быстро падает, они "утомляются
" вследствие поляризации. Только через некоторое время происходит окисление водорода пиролюзитом. Таким образом, элементы "отдыхают
", если некоторое время не пропускать ток. Проверим это на батарейке для карманного фонарика, к которой подсоединим лампочку. Параллельно лампе, то есть непосредственно на клеммы, подключим вольтметр.
Сначала напряжение составит около 4,5 В. (Чаще всего в таких батарейках последовательно включены три ячейки, каждая с теоретическим напряжением 1,48 В.) Через некоторое время напряжение упадет, накал лампочки ослабеет. По показаниям вольтметра мы сможет судить, как долго батарейке нужно отдыхать.
Особое место занимают регенерирующие элементы, известные под названием аккумуляторы
. В них протекают обратимые реакции, и их можно перезаряжать после разрядки элемента, подключив к внешнему источнику постоянного тока.
В настоящее время наиболее распространены свинцовые аккумуляторы; в них электролитом служит разбавленная серная кислота, куда погружены две свинцовые пластины. Положительный электрод покрыт диоксидом свинца PbO 2 , отрицательный представляет собой металлический свинец. Напряжение на клеммах составляет примерно 2,1 В. При разрядке на обеих пластинах образуется сульфат свинца, который опять превращается при зарядке в металлический свинец и в пероксид свинца.
НАНЕСЕНИЕ ГАЛЬВАНИЧЕСКИХ ПОКРЫТИЙ
Осаждение металлов из водных растворов с помощью электрического тока является процессом, обратным электролитическому растворению, с которым мы познакомились при рассмотрении гальванических элементов. Прежде всего исследуем осаждение меди, которое используют в медном кулонометре для измерения количества электричества.Металл осаждается током
Отогнув концы двух пластин из тонкой листовой меди, подвесим их на противоположных стенках химического стакана или, лучше, маленького стеклянного аквариума. Клеммами прикрепим к пластинам провода.
Электролит
приготовим по следующему рецепту: 125 г кристаллического сульфата меди, 50 г концентрированной серной кислоты и 50 г спирта (денатурата), остальное - вода до 1 литра. Для этого сначала растворим сульфат меди в 500 мл воды, затем осторожно, маленькими порциями добавим серную кислоту (Нагревание! Жидкость может разбрызгиваться!
), после этого вольем спирт и доведем водой до объема 1 л.
Готовым раствором наполним кулонометр и включим в цепь переменное сопротивление, амперметр и свинцовый аккумулятор. С помощью сопротивления отрегулируем ток таким образом, чтобы его плотность составила 0,02-0,01 А/см 2 поверхности электродов. Если медная пластина имеет площадь 50 см 2 , то сила тока должна находиться в пределах 0,5-1 А.
Через некоторое время на катоде (отрицательный электрод) начнет выделяться светло-красная металлическая медь, а на аноде (положительный электрод) медь будет переходить в раствор. Чтобы очистить медные пластины, будем пропускать ток в кулонометре около получаса. Затем вытащим катод, осторожно высушим его с помощью фильтровальной бумаги и точно взвесим. Установим в ячейке электрод, замкнем цепь с помощью реостата и будем поддерживать постоянную силу тока, например 1 А. Через час разомкнем цепь и опять взвесим высушенный катод. При токе 1 А за час работы его масса увеличится на 1,18 г.
Следовательно, количество электричества, равное 1 ампер-часу, при прохождении через раствор может выделить 1,18 г меди. Или в общем: выделившееся количество вещества прямо пропорционально количеству прошедшего через раствор электричества.
Чтобы выделить 1 эквивалент иона, необходимо пропустить через раствор количество электричества, равное произведению заряда электрода е на число Авогадро N
A:
е*N
A = 1,6021 * 10 -19 * 6,0225*10 23 = 9,65*10 4 А*с*моль -1
Эта величина обозначается символом F
и называется в честь первооткрывателя количественных законов электролиза числом Фарадея
(точное значение F
- 96 498 А*с*моль -1). Следовательно, для выделения из раствора данного числа эквивалентов n
э через раствор следует пропустить количество электричества, равное F*n
э А*с*моль -1 .
Иначе говоря,
I*t
= F*n
э
Здесь I
- ток, t
- время прохождения тока через раствор.
В разделе "Основы титрования
" уже было показано, что число эквивалентов вещества n
э равно произведению числа молей на эквивалентное число:
n
э = n
*Z
Следовательно:
I *t = F*n*Z
В данном случае Z - заряд ионов (для Ag + Z = 1, для Cu 2+ Z = 2, для Al 3+ Z = 3 и т. д.). Если выразить число молей в виде отношения массы к мольной массе (n = m / М ), то мы получим формулу, которая позволяет рассчитать все процессы, происходящие при электролизе:
I*t = F*m*Z / M
По этой формуле можно вычислить ток:
I = F*m*Z/(t*M) = 9,65*10 4 *1,18*2 / (3600*63,54) А*с*г*моль/(с*моль*г) = 0,996 А
Если ввести соотношение для электрической работы W эл
W эл = U*I*t и W эл /U = I*t
То, зная напряжение U , можно вычислить:
W эл = F*m*Z*U/M
Можно также рассчитать, сколько времени необходимо для электролитического выделения определенного количества вещества или сколько вещества выделится за определенное время.
Во время опыта плотность тока необходимо поддерживать в заданных пределах. Если она будет меньше 0,01 А/см 2 , то выделится слишком мало металла, так как будут частично образовываться ионы меди(I). При слишком высокой плотности тока сцепление покрытия с электродом будет слабым и при извлечении электрода из раствора оно может осыпаться.
На практике гальванические покрытия на металлах применяют прежде всего для защиты от коррозии и для получения зеркального блеска.
Кроме того, металлы, особенно медь и свинец, очищают с помощью анодного растворения и последующего выделения на катоде (электролитическое рафинирование).
Чтобы покрыть железо медью или никелем, необходимо сначала тщательно очистить поверхность предмета. Для этого отполируем ее отмученным мелом и последовательно обезжирим разбавленным раствором едкого натра, водой и спиртом. Если предмет покрыт ржавчиной, надо протравить его заранее в 10-15%-ном растворе серной кислоты.
Очищенное изделие подвесим в электролитической ванне (маленький аквариум или химический стакан), где оно будет служить в качестве катода.
Раствор для нанесения медного покрытия содержит в 1 л воды 250 г сульфата меди и 80-100 г концентрированной серной кислоты (Осторожно!
). В данном случае анодом будет служить медная пластинка. Поверхность анода примерно должна быть равна поверхности покрываемого предмета. Поэтому надо всегда следить, чтобы медный анод висел в ванне на такой же глубине, как и катод.
Процесс будем проводить при напряжении 3-4 В (две аккумуляторные батареи) и плотности тока 0,02-0,4 А/см 2 . Температура раствора в ванне должна составлять 18-25 °С.
Обратим внимание на то, чтобы плоскость анода и покрываемая поверхность были параллельны друг другу. Предметы сложной формы лучше не использовать. Варьируя длительность электролиза, можно получать медное покрытие разной толщины.
Часто прибегают к предварительному меднению для того, чтобы на этот слой нанести прочное покрытие из другого металла. Особенно часто это применяется при хромировании железа, никелировании цинкового литья и в других случаях. Правда, для этой цели используют очень ядовитые цианидные электролиты.
Для приготовления электролита для никелирования в 450 мл воды растворим 25 г кристаллического сульфата никеля, 10 г борной кислоты или 10 г цитрата натрия. Цитрат натрия можно приготовить самим, нейтрализовав раствор 10 г лимонной кислоты разбавленным раствором едкого натра или раствором соды. Анодом пусть будет пластина никеля возможно большей площади, а в качестве источника напряжения возьмем аккумулятор.
Величину плотности тока с помощью переменного сопротивления будем поддерживать равной 0,005 А/см 2 . Например, при поверхности предмета 20 см 2 надо работать при силе тока 0,1 А. После получаса работы предмет будет уже отникелирован. Вытащим его из ванны и протрем тканью. Впрочем, процесс никелирования лучше не прерывать, так как тогда слой никеля может запассивироваться и последующее никелевое покрытие будет плохо держаться.
Чтобы достичь зеркального блеска без механической полировки, введем в гальваническую ванну так называемую блескообразующую добавку. Такими добавками служат, например, клей, желатина, сахар. Можно ввести в никелевую ванну, например, несколько граммов сахара и изучить его действие.
Чтобы приготовить электролит для хромирования железа (после предварительного меднения), в 100 мл воды растворим 40 г ангидрида хромовой кислоты СrО 3 (Осторожно! Яд!
) и точно 0,5 г серной кислоты (ни в коем случае не больше!). Процесс протекает при плотности тока около 0,1 А/см 2 , а в качестве анода используется свинцовая пластина, площадь которой должна быть несколько меньше площади хромируемой поверхности.
Никелевые и хромовые ванны лучше всего слегка подогреть (примерно до 35 °С). Обратим внимание на то, что электролиты для хромирования, особенно при длительном процессе и высокой силе тока, выделяют содержащие хромовую кислоту пары, которые очень вредны для здоровья. Поэтому хромирование следует проводить под тягой или на открытом воздухе, например на балконе.
При хромировании (а в меньшей степени и при никелировали) не весь ток используется на осаждение металла. Одновременно выделяется водород. На основании ряда напряжений следовало бы ожидать, что металлы, стоящие перед водородом, вообще не должны выделяться из водных растворов, а напротив должен был бы выделяться менее активный водород. Однако здесь, как и при анодном растворении металлов, катодное выделение водорода часто тормозится и наблюдается только при высоком напряжении. Это явление называют перенапряжением водорода, и оно особенно велико, например, на свинце. Благодаря этому обстоятельству может функционировать свинцовый аккумулятор. При зарядке аккумулятора вместо РbО 2 на катоде должен бы возникать водород, но, благодаря перенапряжению, выделение водорода начинается тогда, когда аккумулятор почти полностью заряжен.